-
Property & Casualty
Property & Casualty Overview

Property & Casualty
We offer a full range of reinsurance products and the expertise of our talented reinsurance team.
Expertise
Publication
Structured Settlements – What They Are and Why They Matter
Publication
PFAS Awareness and Concern Continues to Grow. Will the Litigation it Generates Do Likewise?
Publication
“Weather” or Not to Use a Forensic Meteorologist in the Claims Process – It’s Not as Expensive as You Think
Publication
Phthalates – Why Now and Should We Be Worried?
Publication
The Hidden Costs of Convenience – The Impact of Food Delivery Apps on Auto Accidents
Publication
That’s a Robotaxi in Your Rear-View Mirror – What Does This Mean for Insurers? -
Life & Health
Life & Health Overview

Life & Health
We offer a full range of reinsurance products and the expertise of our talented reinsurance team.

Publication
Key Takeaways From Our U.S. Claims Fraud Survey
Publication
Favorite Findings – Behavioral Economics and Insurance
Publication
Individual Life Accelerated Underwriting – Highlights of 2024 U.S. Survey
Publication
Can a Low-Price Strategy be Successful in Today’s Competitive Medicare Supplement Market? U.S. Industry Events
U.S. Industry Events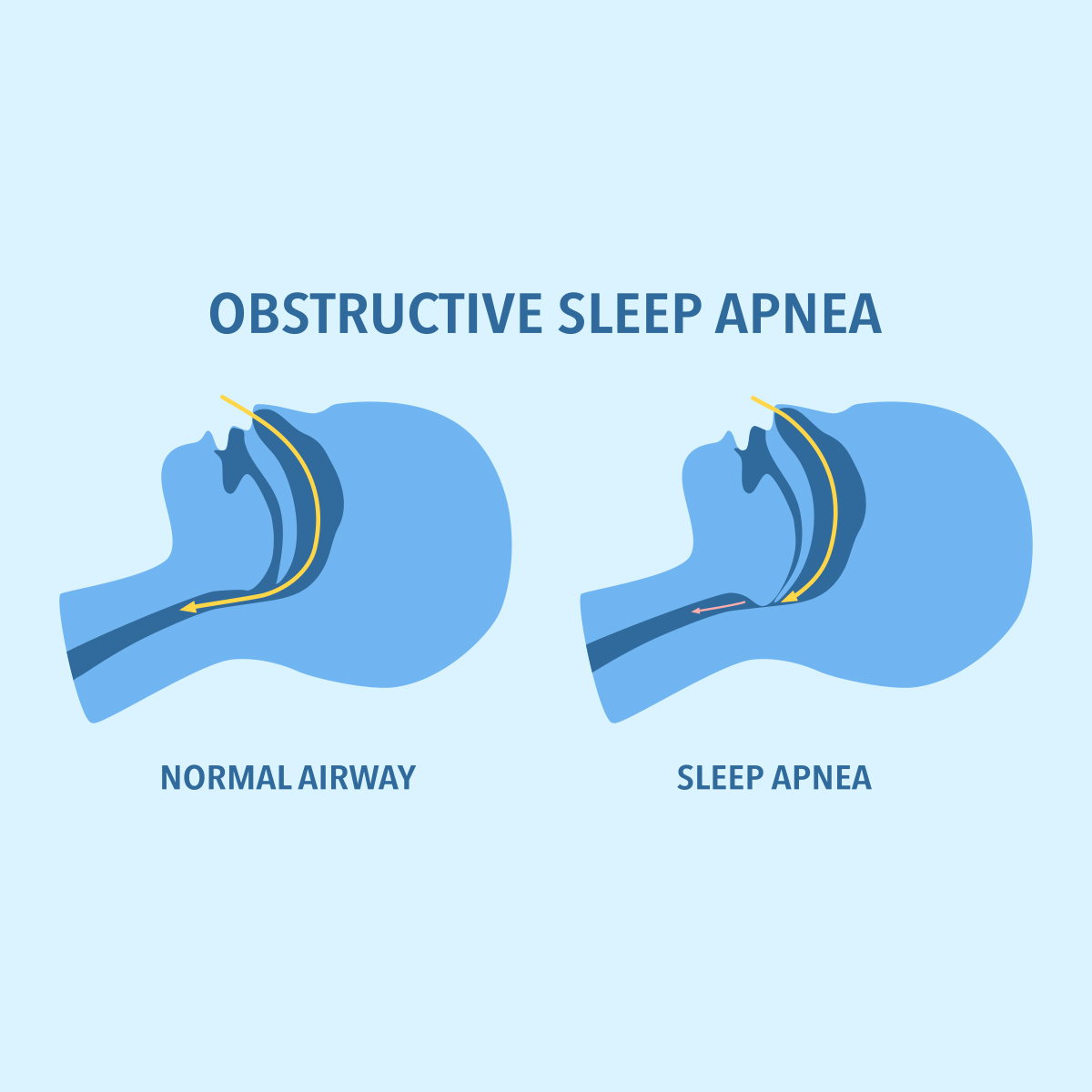
Publication
The Latest in Obstructive Sleep Apnea -
Knowledge Center
Knowledge Center Overview

Knowledge Center
Our global experts share their insights on insurance industry topics.
Trending Topics -
About Us
About Us OverviewCorporate Information

Meet Gen Re
Gen Re delivers reinsurance solutions to the Life & Health and Property & Casualty insurance industries.
- Careers Careers
¿Son las pruebas epigenéticas el futuro de la suscripción de seguros de Vida y Salud?

Las aseguradoras de Vida y Salud están intentando agilizar el proceso de solicitud haciendo el menor número de preguntas posible. Entre las nuevas tecnologías que se están explorando para ayudar a determinar a ciencia cierta el estado de salud de un solicitante, hay una técnica conocida como pruebas epigenéticas.
La epigenética es un campo de la biología molecular que está experimentando una evolución vertiginosa y cuyo objetivo es entender cómo se ve afectada la expresión de los genes por los cambios ambientales. Sin embargo, la epigenética no es lo mismo que la genética. La epigenética describe los procesos reversibles y hereditarios que regulan la función de los genes sin alterar la secuencia primaria del ADN.1
La genética es el estudio de los rasgos hereditarios codificados en el ADN de los individuos. A diferencia de la genética, la epigenética se centra en los cambios reversibles con el tiempo y está influida por multitud de factores ambientales, como el tabaquismo.2,3
Para las aseguradoras es importante saber que ciertas marcas epigenéticas pueden reflejar la rapidez con la que está envejeciendo una persona y, por consiguiente, durante cuánto tiempo se mantendrá sana. Algunos factores de riesgo relevantes para la suscripción de seguros podrían estar vinculados a la epigenética, como el IMC, el tabaquismo, el consumo de alcohol e incluso algunas enfermedades como la diabetes tipo 2 y el cáncer de mama.
Pero ¿se puede sustituir la suscripción de pólizas por un simple test epigenético de saliva? Varios estudios muestran una relación entre los resultados epigenéticos, como los patrones diferentes de metilación del ADN, y ciertos aspectos de los hábitos de los individuos. Sin embargo, para decidir si los test epigenéticos pueden servir de ayuda en el proceso de valoración de riesgos, primero necesitamos saber qué factores de riesgo pueden detectarse de forma fiable mediante de la epigenética.
Envejecimiento
La edad es una de las preguntas básicas que se formulan en cualquier solicitud de seguro, y ciertas preguntas podrían eliminarse utilizando el análisis epigenético. Por ejemplo, algunas marcas epigenéticas (p. ej. el DNAmGrimAge) pueden utilizarse para predecir la edad basándose en una muestra biológica del solicitante.4 Dicha muestra puede ser la saliva, ya que contiene suficiente ADN de alta calidad adecuado para la evaluación del DNAmAge.5
La epigenética es capaz de predecir una serie de relojes epigenéticos que a su vez predicen la edad cronológica del individuo (el tiempo transcurrido desde su nacimiento), la edad biológica (el deterioro de las funciones biológicas) y la edad acelerada (la diferencia entre la edad cronológica y la biológica).6,7 Sin embargo, el uso de relojes epigenéticos como herramienta en la suscripción de pólizas tiene limitaciones, ya que hay en marcha ensayos clínicos que intentan optimizar su eficacia, eficiencia, escalabilidad y asequibilidad.8
Índice de masa corporal (IMC)
La obesidad es una de las principales causas de enfermedades como las cardíacas y el cáncer. Un estudio de 2021 ha revelado que la obesidad puede alterar la metilación del ADN y que dicha alteración puede afectar a la inflamación y a los niveles de lipoproteínas en individuos obesos.9
Otro estudio analizó la relación entre la obesidad y la metilación del ADN en 991 individuos sanos, lo que demuestra la importancia de la epigenética como herramienta de diagnóstico de la obesidad y el riesgo de ciertas enfermedades asociadas a un IMC anormal, así como sus posibles consecuencias.10 La metilación del ADN relacionada con el IMC se ha estudiado a fondo y demuestra ser relevante para desarrollar enfermedades cardiometabólicas relacionadas con la obesidad.11 Dado que se observan patrones particulares de metilación en el contexto de la obesidad, esta información podría ser útil para valorar el riesgo de los solicitantes con un IMC alto.
Tabaquismo
Diversos estudios han revelado que el tabaquismo provoca cambios generalizados en la epigenética del individuo a través de alteraciones en el patrón de la metilación del ADN.12 Por ejemplo, se ha demostrado que la metilación de cg05575921 (un sitio específico de CpG) disminuye con el tabaquismo.13,14 Por lo tanto, la identificación de cambios en estos loci genéticos relacionados con el tabaquismo también indicaría – en teoría – el estado de tabaquismo de un individuo.
Como ocurre con otros cambios epigenéticos, la metilación del ADN inducida por el tabaco es reversible, y un estudio demostró que la comparación entre los niveles de metilación de los loci de interés antes mencionados entre personas que nunca han fumado y exfumadores ha mostrado muy poca o ninguna diferencia cinco años después de haber dejado de fumar.15 Por consiguiente, confiar solo en la información epigenética podría ocultar a los antiguos fumadores empedernidos, dando lugar a una selección negativa.
Además, dejar de fumar supuestamente permite recuperar el estado de metilación del ADN de las personas que nunca han fumado. No obstante, esto sigue dependiendo del tiempo transcurrido desde que la persona dejara de fumar y el índice de cajetillas por año de esos exfumadores.16 Aunque algunos estudios han relacionado la intensidad del tabaquismo con los niveles de metilación del ADN, en su mayoría se han realizado en ratones o solo en pequeñas muestras de ADN de sangre total humana o ADN de saliva. Se necesitan más datos para tener una mayor seguridad sobre la correlación entre los cambios epigenéticos en los loci y fumar o incluso vapear.17
Consumo de alcohol
Si fuera posible hacer un sencillo test epigenético de saliva para detectar un comportamiento pasado de adicción o consumo abusivo de alcohol, ¿por qué no utilizar la epigenética para la suscripción? Varios estudios han revelado la vinculación entre ciertos patrones de metilación del ADN con la dependencia del alcohol.18,19
Se sabe que ciertos cambios de en el estilo de vida podrían cambiar la metilación del ADN, y esto también se ha observado en los consumidores de alcohol. Además, un estudio de 2018 reveló que el ejercicio diario fue capaz de invertir en sentido positivo la metilación del ADN en bebedores de riesgo y bebedores compulsivos, por lo que podría ser una forma de prevenir el abuso de alcohol.20
Diabetes tipo 2
La diabetes tipo 2 es una comorbilidad frecuente, sobre todo entre la población obesa. También es responsable de multitud de efectos negativos sobre la salud, como enfermedades cardiovasculares, y en la suscripción de riesgos se analiza a fondo. Algunos estudios han detectado diferencias en el patrón epigenético (p. ej. metilación del ADN y expresión genética) en las células sanguíneas, la musculatura esquelética, el tejido adiposo, el hígado y los islotes pancreáticos de personas con diabetes tipo 2 en comparación con los controles no diabéticos.21
Es importante señalar que los patrones epigenéticos son específicos de las células y los tejidos. Para conocer a fondo el estado diabético de un individuo, se necesitan muestras epigenéticas de los tejidos relevantes para la enfermedad. A los efectos de la suscripción de seguros, la obtención de estas muestras específicas de tejido, además de sangre o saliva, para obtener un patrón epigenético más preciso de enfermedades como la diabetes tipo 2 y la obesidad no resulta muy práctica.
Cáncer de mama
En la actualidad, se utilizan distintos patrones de metilación del ADN para estratificar el riesgo en el cáncer de mama, y su vinculación se ha analizado en diversos estudios.22 La trimetilación de la lisina 27 de la histona H3 (H3 K27 me) es una marca epigenética que ha demostrado su capacidad para predecir la supervivencia del cáncer. Se ha observado que la expresión de H3 K27 me3 en los tejidos con cáncer de mama es significativamente menor que en los tejidos normales. Además, se observó que los individuos con cáncer de mama y una menor expresión de H3 K27 me3 tenían una tasa de supervivencia global significativamente más corta que los individuos con una expresión mayor.23
Al comparar la metilación del tejido mamario normal con el carcinoma ductal in situ y el carcinoma invasivo de mama, la metilación del ADN estaba muy alterada en 5.000 genes del tejido mamario in situ. Por su parte, aproximadamente 1.000 genes estaban alterados en el carcinoma invasivo de mama. Esto sugiere que la metilación del ADN se podría usar como biomarcador incluso en las primeras fases del cáncer de mama.24
Es importante señalar que otros metaanálisis no muestran una vinculación entre ciertos niveles de metilación del ADN y un mayor riesgo de cáncer de mama o de supervivencia al cáncer de mama.25 Por tanto, los resultados científicos aún no son lo suficientemente concluyentes como para determinar si las aseguradoras deben utilizar la información epigenética para predecir la supervivencia o el riesgo de los pacientes con cáncer de mama basándose únicamente en la información epigenética.
Cuestiones sociales y morales
En el ámbito de la epigenética, un sencillo test de saliva o sangre ofrece información sobre si la expresión genética de una persona ha cambiado debido a ciertos hábitos o alteraciones ambientales. En la suscripción de seguros, para ciertas enfermedades necesitamos valores de laboratorio a fin de comprobar el estado de salud del solicitante. Está claro desde el principio qué valores de laboratorio se necesitan. El uso de la epigenética podría significar que los solicitantes de pólizas reciban nueva información sobre su salud que de otro modo habrían preferido mantener privada. Además, así un tercero ha recibido información que podría ser desfavorable y no estaba destinada a hacerse pública: la información inesperada procedente de la epigenética podría dar lugar a casos de discriminación o dificultar que se ignoren los factores desfavorables.26
Si un test revela determinados factores desfavorables, ¿cómo se debe informar del resultado a la persona? ¿Pueden las aseguradoras utilizar esta información que antes se desconocía y hacerlo también a efectos de suscripción de riesgos? El campo de la epigenética está aún en pañales y quedan muchos retos por delante; los mecanismos epigenéticos son en su mayoría poco conocidos y aislar un único factor ambiental sigue siendo un problema. Además, los pocos estudios disponibles se limitan a un número reducido de participantes y a poblaciones específicas, lo que reduce la potencia estadística de los resultados. Por tanto, es muy importante que se siga estudiando y analizando la fiabilidad científica de la epigenética para garantizar su validez, sobre todo si se quiere utilizar información basada en evidencia sobre epigenética como base sólida para los seguros y la suscripción de pólizas.
- Berdasco, M., & Esteller, M. (2019). Clinical epigenetics: Seizing opportunities for translation. Nature Reviews. Genetics, 20 (2), 109‑127.
- Center for Disease Control and Prevention. (2022). What is epigenetics? https://www.cdc.gov/genomics/disease/epigenetics.htm.
- Philibert, R., Mills, J. A., Long, J. D., et al. (2020). The reversion of cg05575921 methylation in smoking cessation: A potential tool for incentivizing healthy aging. Genes, 11 (12), 1415.
- Lu, A. T., Quach, A., Wilson, J. G., et al. (2019). DNA methylation GrimAge strongly predicts lifespan and healthspan. Aging, 11 (2), 303‑327.
- Fitzgerald, K. N., Hodges, R., Hanes, D., et al. (2021). Potential reversal of epigenetic age using a diet and lifestyle intervention: A pilot randomized clinical trial. Aging, 13 (7), 9419‑9432.
- Topart, C., Werner, E., & Arimondo, P. B. (2020). Wandering along the epigenetic timeline. Clinical Epigenetics, 12 (1), 97.
- Li, A., Koch, Z., & Ideker, T. (2022). Epigenetic aging: Biological age prediction and informing a mechanistic theory of aging. Journal of Internal Medicine, 292 (5), 733‑744.
- Ibid, see endnote 5.
- Chen, Y., Kassam, I., Lau, S. H., et al. (2021). Impact of BMI and waist circumference on epigenome-wide DNA methylation and identification of epigenetic biomarkers in blood: An EWAS in multi-ethnic Asian individuals. Clinical Epigenetics, 13 (1), 195.
- Aslibekyan, S., Demerath, E. W., Mendelson, M., et al. (2015). Epigenome-wide study identifies novel methylation loci associated with body mass index and waist circumference. Obesity (Silver Spring, Md.), 23 (7), 1493‑1501.
- Mendelson, M. M., Marioni, R. E., Joehanes, R., et al. (2017). Association of body mass index with DNA methylation and gene expression in blood cells and relations to cardiometabolic disease: A Mendelian randomization approach. PLoS Medicine, 14 (1), e1002215.
- Zeilinger, S., Kühnel, B., Klopp, N., et al. (2013). Tobacco smoking leads to extensive genome-wide changes in DNA methylation. PloS One, 8 (5), e63812.
- Dawes, K., Andersen, A., Reimer, R., et al. (2021). The relationship of smoking to cg05575921 methylation in blood and saliva DNA samples from several studies. Scientific Reports, 11 (1), 21627.
- Ibid, see endnote 3.
- Joehanes, R., Just, A. C., Marioni, R. E., et al. (2016). Epigenetic signatures of cigarette smoking. Circulation Cardiovascular Genetics, 9 (5), 436‑447.
- Ibid, see endnote 10.
- Xie, Z., Rahman, I., Goniewicz, M. L., & Li, D. (2021). Perspectives on epigenetics alterations associated with smoking and vaping. Function (Oxford, England), 2(3), zqab022.
- Ciafrè, S., Carito, V., Ferraguti, G., et al. (2019). How alcohol drinking affects our genes: An epigenetic point of view. Biochemistry and Cell Biology, 97 (4), 345‑356.
- Liu, C., Marioni, R. E., Hedman, Å. K., et al. (2018). A DNA methylation biomarker of alcohol consumption. Molecular Psychiatry, 23 (2), 422‑433.
- Chen, J., Hutchison, K. E., Bryan, A. D., et al. (2018). Opposite epigenetic associations with alcohol use and exercise intervention. Frontiers in Psychiatry, 9, 594.
- Ling, C., & Rönn, T. (2019). Epigenetics in human obesity and type 2 diabetes. Cell Metabolism, 29 (5), 1028‑1044.
- Wei, Y., Xia, W., Zhang, Z., et al. (2008). Loss of trimethylation at lysine 27 of histone H3 is a predictor of poor outcome in breast, ovarian, and pancreatic cancers. Molecular Carcinogenesis, 47 (9), 701‑706.
- Ibid.
- Fleischer, T., Frigessi, A., Johnson, K. C., et al. (2014). Genome-wide DNA methylation profiles in progression to in situ and invasive carcinoma of the breast with impact on gene transcription and prognosis. Genome Biology, 15 (8), 435.
- Bodelon, C., Ambatipudi, S., Dugué, P. A., et al. (2019). Blood DNA methylation and breast cancer risk: A meta-analysis of four prospective cohort studies. Breast Cancer Research: BCR, 21 (1), 62.
- Dupras, C., Song, L., Saulnier, K. M., & Joly, Y. (2018). Epigenetic discrimination: Emerging applications of epigenetics pointing to the limitations of policies against genetic discrimination. Frontiers in Genetics, 9, 202.
All endnotes last accessed on 4 December 2023.






